医疗检测系统设计
医疗器械研发阶段的质量管理计划是确保产品设计、开发和生产过程中始终保持高质量标准的重点策略。该计划明确了质量目标、原则和方法,并贯穿于整个研发流程。团队需建立严格的质量控制体系,包括制定详细的质量标准、进行定期的质量检查与评估,以及及时处理质量问题。同时,质量管理计划强调预防原则,通过风险评估和持续改进,减少潜在质量问题的发生。有效执行质量管理计划不仅能提升医疗器械的安全性和有效性,还能提高生产效率,降低成本,为产品的市场竞争力和用户满意度奠定坚实基础。医疗器械研发需要关注产品的可持续性,减少对环境的影响。医疗检测系统设计
自2018年注册人制度在上海自贸区开展以来,已经在全国落地开花,并取得了良好的效果。如今火热的内窥镜市场,已经从外企的一家独大变为国产逐渐替代,每年都有许多国产产品获准上市,这充分说明了注册人制度的有效性。尽管注册人制度有许多优点,但也面临着一些挑战。例如,注册人需要对产品的全生命周期质量负责,这需要他们具备足够的质量控制能力和风险管理能力。此外,跨区域监管也是一个需要解决的问题。总的来说,医疗器械研发与注册人制度是相互促进、相互制约的两个过程。只有充分理解和掌握这两个过程,才能更好地推动医疗器械行业的发展。全套医疗器械设计开发开发内容用户体验在医疗器械研发中至关重要,直接影响产品的市场接受度。

医疗器械研发的输出阶段是研发过程中的重要环节,主要包括设计与开发输入评审、设计与开发输出评审、设计与开发验证评审、设计与开发确认评审以及设计与开发转换评审。这些阶段的目标是确保产品设计和开发过程符合法规和标准,同时满足用户和市场需求。每个阶段都有特定的目标和任务,需要按照规定的流程和标准进行操作,以确保产品的质量和安全性。思脉得医疗科技技术开发团队凭借过硬的技术储备和专业知识,可以提供指导服务,帮助客户确认设计的合理性。
医疗器械研发阶段的持续改进策略是确保产品质量不断提升、满足市场需求和法规要求的重点方法。该策略强调在研发过程中持续识别问题、分析原因,并采取有效措施进行改进。团队需建立反馈机制,及时收集研发各阶段的数据和意见,评估产品性能和用户满意度。通过持续改进设计、材料选择、生产工艺等方面,提高医疗器械的安全性、有效性和可靠性。同时,关注法规和标准的更新,及时调整产品设计和研发流程,确保持续符合法规要求。持续改进策略的实施有助于医疗器械研发团队不断优化产品,提升市场竞争力,并为患者带来更安全、高效的医疗解决方案。医疗器械研发中的伦理审查和监管是确保产品符合道德和法律要求的重要环节。

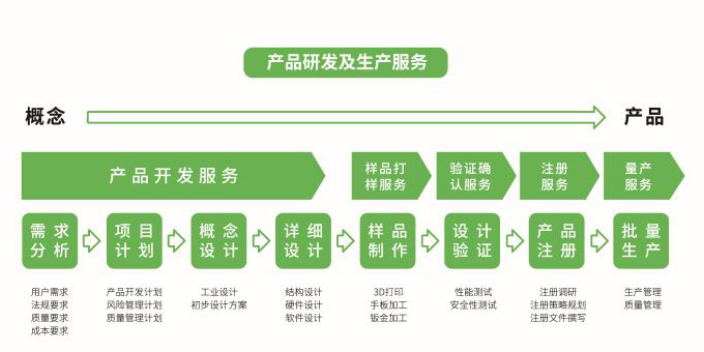
医疗器械的生命周期包括需求分析、设计、生产、流通、使用、维护和退市等阶段。在需求分析阶段,团队根据市场需求和医学需求确定产品方向. 设计阶段包括外观设计、结构设计、功能设计和临床试验、生产阶段涉及原材料采购、生产工艺流程设计和质量控制。流通阶段包括运输、仓储和销售。使用阶段涉及医院、诊所和个人消费者,需要按照说明书正确使用并进行定期维护。维护阶段包括维修、保养和升级。退市阶段,企业根据产品销售情况和市场需求决定是否停止生产和销售。医疗器械研发中的用户体验设计有助于提升产品的整体满意度和忠诚度。医疗检测系统设计
注塑技术的应用提升了医疗器械的制造效率。医疗检测系统设计
医疗器械的合规性是企业在研发、生产、销售等环节中必须严格遵守的一系列法规和标准。这不仅是为了保护消费者的权益,也是企业自身生存和发展的关键。在医疗器械的研发过程中,合规性是产品能否成功上市的关键因素之一。企业在研发过程中需要遵循一系列的法规标准,如ISO 13485,这是设计与开发的基础标准,产品设计开发流程、合规性保证等都是其重要内容。在医疗器械的销售环节,也需要遵循一系列的法规标准。例如,医疗器械网络销售的立法沿革与监管框架,自2005年以来,我国有序地放开了医疗器械的网络销售模式,但在监管方式上,以事前审查验收制度提出对医疗器械网络销售的严格要求。医疗检测系统设计
上一篇: 深圳医疗器械设计开发优化
下一篇: 成都医疗器械设计