广东医疗器械设计开发值得推荐
医疗器械研发阶段的生物相容性是确保器械安全有效应用于人体的关键环节。它指的是医疗器械与人体组织、细胞及生物系统之间的相互作用,要求器械在接触人体时不会引起毒性、过敏、炎症等不良反应。为确保生物相容性,研发阶段需进行严格的材料筛选、生物相容性测试和评估。这包括选择符合生物安全标准的材料,通过体外和体内试验验证材料的生物相容性,以及评估器械在人体内的长期安全性和有效性。同时,研发团队还需密切关注人体对器械的免疫反应和生物降解等因素,确保器械在人体内具有良好的耐受性和功能性。因此,医疗器械研发阶段的生物相容性是保障患者安全和器械性能的重要考量,也是推动医疗器械创新发展的基础。医疗器械研发中的标准化和模块化设计有助于提高生产效率和降低成本。广东医疗器械设计开发值得推荐

医疗器械研发阶段的医疗器械安全性评估是确保器械在使用过程中不会对患者或使用者造成伤害的关键步骤。评估过程涉及对器械设计、材料、制造工艺以及预期用途的多角度分析,以确定潜在的安全风险。这包括识别器械可能引发的生物相容性问题、电气安全风险、机械伤害等,并通过一系列严格的测试和验证来评估这些风险的可接受程度。研发团队需确保所有安全性评估均符合相关法规和标准要求,以保证评估结果的准确性和可靠性。此外,安全性评估还需考虑器械在实际使用环境中的性能表现,包括与其他医疗设备的兼容性、操作便捷性等。通过多方面的医疗器械安全性评估,研发团队能够及时发现并解决潜在的安全问题,为器械的顺利上市和广泛应用提供坚实保障。上海国际医疗器械设计与制造技术展览会从概念到实现,医疗器械研发需要经历多个阶段,每个阶段都充满挑战。
评审的主要目的是为了评价设计和开发的结果是否满足预期的要求,同时识别可能出现的问题并提出必要的行动措施。这是确保产品或服务达到预定目标和满足用户需求的关键步骤。评审的过程可以帮助团队发现潜在的问题和风险,从而及时采取措施进行纠正,避免在后期阶段出现更大的问题。评审的另一个重要性在于,它可以帮助团队识别和弥补自身能力的不足。通过邀请组织外的其他人员参与评审,可以提供不同的观点和经验,有助于发现设计和开发过程中可能被忽视的问题。此外,评审还可以确保设计和开发过程的合规性,例如满足相关的法律、法规和标准要求
在设置评审点时,需要考虑产品的风险大小和复杂性,以及设计和开发过程的不同阶段。评审点的设置并不是越多越好,过多的评审点可能会增加管理难度,延长开发周期。相反,如果评审点太少,可能会给设计和开发带来较大的风险,难以保证开发质量。评审人员的选择也是非常重要的。他们应该是具有资格的人员,包括设计和开发阶段的职能负责人、项目团队成员,以及组织外的其他人员,以补充项目团队能力的不足。在评审过程中发现的问题需要及时归零,以确保评审效果。在医疗器械研发中,质量控制是确保产品安全性和有效性的重要环节。
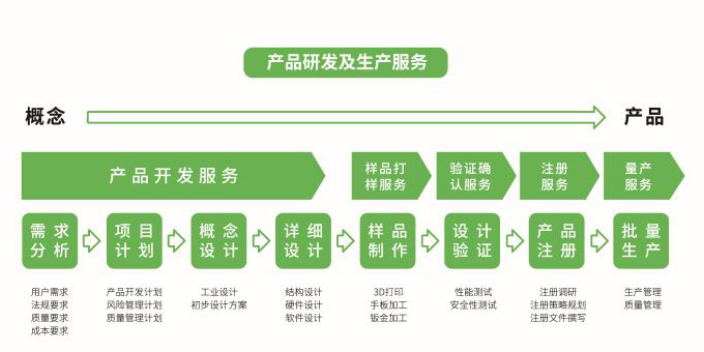
在医疗器械研发阶段,监管工作是至关重要的一环。首先,医疗器械的研发需要遵循一系列严格的法规和标准,如《医疗器械监督管理条例》和《医疗器械注册管理办法》等,这些法规和标准对医疗器械的研发、生产和销售等各个环节都进行了详细的规定。其次,医疗器械的研发过程中还需要进行风险评估,以确保产品的安全性。这个风险评估不仅包括对产品本身的风险评估,还包括对研发过程中的风险评估,如设计风险、制造风险、市场风险等。后期,医疗器械的研发还需要进行严格的监管和审查,以确保产品的质量和安全性。这个监管和审查不仅包括对产品的审查,还包括对研发过程的审查,如研发计划的审查、研发结果的审查等。总的来说,医疗器械的研发阶段的监管工作是非常重要和复杂的,需要研发团队严格遵循相关的法规和标准,进行严格的风险评估和审查,以确保产品的质量和安全性。医疗器械研发中的数据分析有助于了解用户行为和市场需求,为产品改进提供依据。医院设备设计
医疗器械研发需要关注产品的兼容性和互操作性,以便与其他设备配合使用。广东医疗器械设计开发值得推荐
医疗器械研发阶段的风险管理计划是确保研发过程顺利进行并很大程度降低潜在风险的关键策略。该计划通过系统识别、评估、控制和监控研发过程中可能出现的风险,确保产品安全性、有效性和质量。在制定风险管理计划时,团队需考虑技术难题、市场需求变化、法规调整等多方面因素,制定相应的风险应对措施。通过定期审查和调整风险管理计划,团队能及时发现新风险并采取措施,确保研发工作的顺利进行。有效的风险管理计划不仅能提升医疗器械研发的成功率,还能保障患者安全,增强产品市场竞争力。广东医疗器械设计开发值得推荐
上一篇: 加工医疗器械
下一篇: 医疗器械CRO服务平台